【政策解读】《药品现代物流规范化建设指导意见》发布,物流合规迎来统一新时代

医药行业从业者注意了!2026年3月20日,国家药监局正式印发《药品现代物流规范化建设指导意见》(以下简称《意见》),并于3月25日对外公布,自发布之日起正式施行[2]。
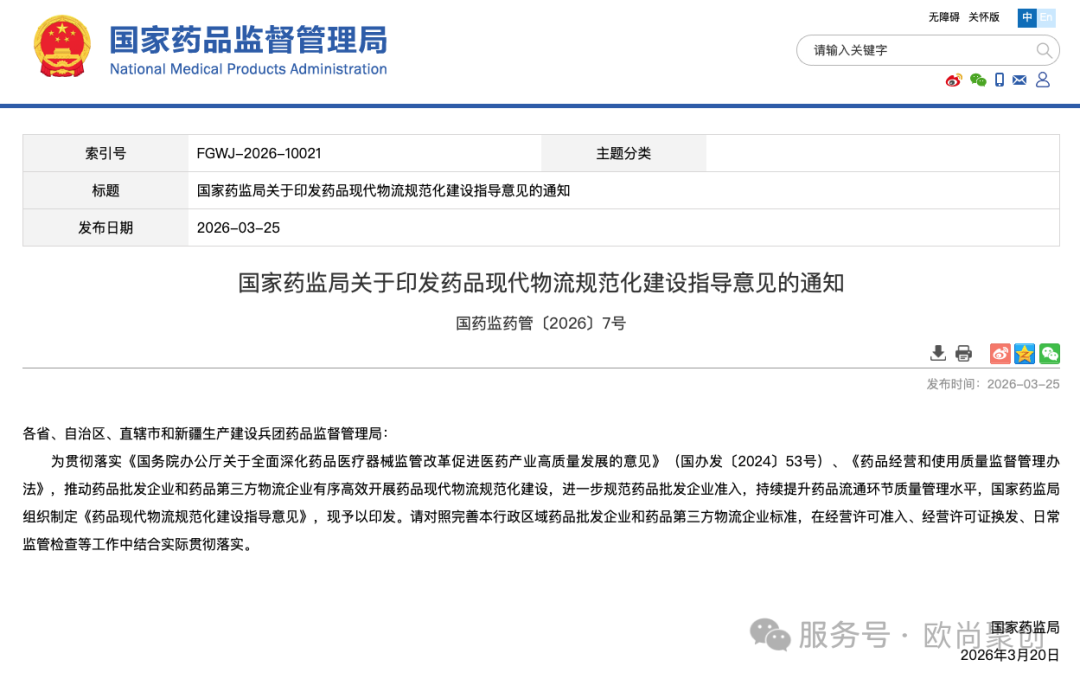
作为药品现代物流领域的顶层设计文件,《意见》统一了全国药品现代物流技术标准,明确了药品批发企业与第三方物流企业的建设要求,将深刻影响整个医药流通行业的合规布局与发展方向。
本文将从政策背景、核心要点、行业影响、落地建议四大维度,为大家全面拆解这份重磅文件,帮你快速理清政策要求、规避合规风险、把握发展机遇。
一、政策出台:为何此时出台这份“纲领性文件”?
在《意见》出台前,我国药品现代物流领域已形成一定规模,但长期存在“标准不一、发展不均”的痛点。
一方面,各省(区、市)因经济发展水平、产业规模差异,出台的药品现代物流标准参差不齐[3],导致药品跨区域流通面临技术壁垒,不利于全国统一大市场建设;
另一方面,部分企业物流设施简陋、信息化水平低、追溯体系不完善,存在药品储存运输质量安全隐患。
基于此,为贯彻落实《国务院办公厅关于全面深化药品医疗器械监管改革促进医药产业高质量发展的意见》《药品经营和使用质量监督管理办法》等顶层要求[1][2],国家药监局牵头制定《意见》,核心目标有三:
统一全国标准,打破区域壁垒,推动药品现代物流规模化、集约化发展;
规范企业准入与运营,抬高行业门槛,淘汰低水平物流主体,提升流通环节质量管控水平;
构建全链条可追溯体系,保障药品储存运输安全,切实守护人民群众用药可及性[3][4]。
值得注意的是,《意见》并非强制性法规,而是指导药品现代物流建设的技术文件,但各省药监局将其作为企业经营许可准入、经营许可证换发、日常监管检查的重要依据[4],未达标企业将面临准入限制或整改要求,其实际约束力不容小觑。
二、核心要点:6大维度读懂政策硬要求(必看)
《意见》覆盖药品批发企业(新开办、已运营)和第三方药品现代物流企业,同时为MAHDS、药品生产企业等委托储运行为提供规范指引[2],核心要求集中在人员、仓库、设施、运输、信息、质量6大维度,其中第三方物流企业有额外专项要求,具体如下:
(一)人员与机构:明确资质门槛,强化责任落实
人员是合规运营的核心,《意见》对从业人员的资质、岗位配置提出明确要求,杜绝“无证上岗、责任不清”的问题:
通用要求:企业需设立物流管理机构,配备物流、计算机专职管理人员,需具备大专以上相关专业或国家认可的职业资格;法定代表人、质量负责人需履职到位,无禁业情形,质量负责人对药品质量管理拥有裁决权[2][4]。
第三方物流专项:物流、计算机管理人员各不少于2名,确保专业能力适配多客户、多场景的物流服务需求[2]。
培训要求:物流质量管理、验收、养护、运输等人员需经过药品储运相关法律法规培训,确保掌握合规要求[2]。
(二)仓库与场地:硬指标落地,筑牢储存安全底线
仓库是药品储存的核心载体,《意见》对仓库的选址、布局、功能区域提出明确硬要求,尤其强化了第三方物流企业的规模标准:
通用要求:仓库需为自营合规建筑,无污染源,实现人流、物流严格分开,有效物理隔离;必须设置常温库、阴凉库(10~20℃)、冷库、不合格/退货专用区,满足不同药品的储存需求[2]。
第三方物流专项(强制规模):仓储作业区建筑面积≥10000㎡,整件立体/高架库≥25000m³,零货货位≥3500个;冷链业务需配备≥2个独立冷库,总容积≥500m³,疫苗库需实现“一用一备”[2]。
安全要求:配备防盗、视频监控等设施,普通药品监控记录留存≥30日,特殊药品≥90日[2]。
(三)设施设备:智能化升级,保障作业合规高效
设施设备的标准化、智能化,是提升物流效率、保障药品质量的关键,《意见》明确要求企业配备适配的现代化设备:
基础设备:配备自动化/智能化物流设备(输送线、堆垛机、叉车等)、温湿度调控系统,实现药品入库、分拣、上架、出库等环节的自动化操作[2][6]。
应急保障:必须配备双回路供电或备用发电机,确保冷库、监控、信息系统不停运,避免因断电导致药品质量受损[2][6]。
校准要求:冷库、冷链设备停用超期需重新验证,计量设备需定期校准,确保设备运行精准[2]。
(四)运输管理:全流程管控,强化追溯能力
药品运输是质量管控的薄弱环节,《意见》从车辆配置、运输流程、追溯要求三方面,实现运输环节的全闭环管控:
车辆要求:采用封闭式药品运输车辆;第三方物流企业需配备非冷链车≥10辆、冷藏车≥2辆,冷藏车需具备独立制冷、车载温控、远程传输、卫星定位功能[2]。
委托管理:二次委托运输需经委托方同意,同时对受托方资质进行严格审核,确保运输全流程可追溯[2]。
温控要求:冷链运输需全程监控温湿度,确保药品在规定温区范围内流转,杜绝温控超限风险[2]。
(五)信息系统与数据:数字化闭环,实现全链条追溯
数字化、可追溯是药品现代物流的核心要求,《意见》明确了信息系统的建设标准和数据管理要求,推动物流全流程信息化:
系统要求:构建覆盖全流程的信息系统,实现ERP、仓储管理系统(WMS)、运输管理系统(TMS)、温湿度监测系统、药品追溯系统互联互通[2][5][6],打破信息孤岛。
第三方物流专项:必须建设信息交换平台,实现与委托方指令、数据的实时互通,同时保障多委托方数据严格隔离[2]。
数据管理:数据按日备份、异地/多机热备,普通记录留存≥5年且不少于效期满后1年,确保数据可追溯、可核查[2]。
(六)质量与委托管理:完善制度体系,明确责任边界
质量管理制度是合规运营的基础,《意见》在GSP基础上,新增多项质量管理制度要求,同时明确委托双方的责任边界:
制度要求:新增物流管理、数据管理、网络安全、应急预案、委托储存运输质量评审等制度,构建完善的质量管控体系[2]。
委托管理:第三方物流企业需与委托方签订质量协议,明确质量责任、追溯要求、违约责任,避免责任不清导致的合规风险[2]。
地方衔接:允许各省(区、市)药监局结合本地实际,制定地方实施细则,但地方标准不得低于全国基本要求[4]。
三、行业影响:3大变革,重塑医药物流格局
《意见》的出台,不仅明确了企业合规红线,更将推动医药物流行业迎来新一轮洗牌与升级,核心影响体现在3个方面:
1.统一标准,打破区域壁垒,推动全国统一大市场建设
此前各省药品现代物流标准不一,导致药品跨区域流通面临技术障碍,部分企业需适配不同省份的标准,增加了运营成本[3]。
《意见》出台后,全国药品现代物流有了统一的技术指导标准,将有效打通区域流通壁垒,提升药品跨区域配送效率,推动医药物流集约化发展[4]。
2.抬高行业门槛,加速行业洗牌,淘汰低水平主体
《意见》对仓库规模、设施设备、人员资质、信息化水平等提出明确硬要求,尤其是第三方物流企业的规模门槛,将让一批设施简陋、信息化薄弱、合规能力不足的小型物流企业难以达标,逐步被市场淘汰[4]。而具备规模化、智能化、合规化能力的头部企业,将获得更多市场份额,推动行业向专业化、集约化转型。
3.强化质量管控,规范第三方物流,释放专业服务能力
《意见》首次明确第三方物流企业的专项要求,界定了委托方与受托方的责任边界,将推动药品储运业务的社会化、专业化分工[4]。同时,全链条追溯、温湿度实时监控等要求,将进一步降低药品储存运输过程中的质量风险,保障人民群众用药安全可及[3]。
四、落地建议:企业如何快速适配政策,规避合规风险?
对于医药企业而言,《意见》不是“选择题”,而是“必答题”。结合政策要求,针对不同类型企业,提出以下落地建议,助力企业快速合规达标:
(一)药品批发企业(新开办)
严格按照《意见》要求,从源头规划物流体系:优先落实仓库、设施设备的硬指标,配备符合要求的专业人员,搭建互联互通的信息系统,确保在经营许可准入阶段即可满足合规要求,避免因未达标被驳回申请[2][4]。
(二)药品批发企业(已运营)
对照《意见》要求开展自查自纠,重点排查仓库规模、设施设备、信息系统、人员资质等薄弱环节:对未达标的部分制定升级改造计划,逐步完善质量管理制度和追溯体系,确保在经营许可证换发、日常监管检查中顺利通过核查[2][3]。
(三)第三方药品物流企业
聚焦专项要求,重点强化3点:
一是补齐仓库、车辆等硬指标短板,满足规模化运营要求;
二是搭建信息交换平台,实现与委托方数据实时互通,同时做好数据隔离;
三是完善委托管理流程,与委托方签订规范的质量协议,明确双方责任,提升专业服务能力[2][4]。
(四)全行业通用建议
加强人员培训,确保物流、计算机、质量管理人员熟练掌握政策要求和操作规范;
建立常态化自查机制,定期排查合规风险,及时整改问题;
密切关注地方实施细则,结合本地监管要求,优化物流合规布局[4]。
五、总结:合规为王,拥抱物流现代化新时代
《药品现代物流规范化建设指导意见》的发布,标志着我国药品现代物流行业进入“统一标准、规范发展、质量优先”的新阶段。对于医药企业而言,政策既是约束,更是机遇——严格落实合规要求,不仅能规避监管风险,更能提升物流效率、降低运营成本、增强市场竞争力。
未来,随着政策的逐步落地,医药物流行业将逐步实现规模化、集约化、数字化、智能化、可追溯的发展目标[4],一批具备核心竞争力的物流企业将脱颖而出,推动整个医药流通行业高质量发展。
建议所有医药从业者认真研读《意见》原文,结合企业自身情况,提前布局、主动适配,在合规前提下实现可持续发展。
https://www.nmpa.gov.cn/xxgk/fgwj/gzwj/gzwjyp/20260325162502165.html